

El Pais
News Press Service
JAVIER SAMPEDRO
El alcalde Crockett está nervioso. No es por tener que hablar en público -es el pastor luterano del pueblo desde hace más de 15 años-, sino por los dos hombres que van a hablar después, los que acaban de aterrizar en la avioneta de Fairbanks.
«La gripe española fue cosa seria, amigo, pero lo del plan de preparación contra la gripe aviar… vaya murga», murmura Brian Crockett mientras intenta conectar el micrófono. «Hay que estar preparados. ¿Cuántos han muerto en Irak? ¿Quién estaba preparado para eso? Escuche una cosa, amigo: cuanto más cambian las cosas, más siguen igual. ¿Ha leído usted a Samuel Huntington? Gripe aviar. El proyector de diapositivas no funciona».
La audiencia va llegando a la cancha de la escuela. En 15 minutos, cuando sean unos cien, el alcalde Crockett presentará a los dos insólitos visitantes: un médico retirado y el director de un laboratorio militar de Washington. Para entender qué hacen aquí no tenemos que movernos del sitio, pero sí retrasar el reloj 87 años y sumergirnos de lleno en el horror.
MÁS INFORMACIÓN
El primero del pueblo murió el 15 de noviembre de 1918. La Gran Guerra había acabado justo el día antes, pero es improbable que esa noticia hubiera llegado a Brevig Mission, un poblado de 80 esquimales situado casi exactamente donde la humanidad descubrió América. Esto es, donde la descubrió de verdad: 10.000 años antes que Colón, y 8.000 kilómetros más al norte, en el estrecho de Bering, que apenas separa Siberia de Alaska, junto al círculo polar ártico.
El primer muerto
Aquel 15 de noviembre, cuando murió el primer esquimal, el virus ya se había propagado por medio planeta, alojado en los pulmones de miles de soldados que habían sobrevivido a la artillería sólo para ganarse otra muerte igual de segura, pero retardada unos días, el plazo suficiente para que un par de sargentos de los que no dejan su puesto por un vulgar ataque de tos contagien a media fragata; después, a medio hospital de campaña.
En Brevig Mission hay ahora una clínica atendida por un ATS, pero en 1918 no se había visto allí nada parecido a un hospital de campaña, ni a un sargento, y los 80 esquimales del poblado estuvieron realmente muy cerca de librarse de la gripe española, como se habían librado de aquella remota guerra que había barrido el planeta hasta el día antes.
Pero la gripe viajó más lejos que la guerra. Dicen en Brevig que el virus les llegó por carta, en el trineo que les traía el correo desde Nome. Es posible que el primer esquimal se infectara así, y que después contagiara a los demás al visitarles, o al recibir sus visitas. Lo único seguro es que el virus hizo bien su trabajo. En el cementerio, una cruz algo más alta que las demás deja leer hoy al raro visitante:
«Los siguientes 72 esquimales inupiat están enterrados en esta fosa común. Reza por ellos, honra y recuerda a estos aldeanos que perdieron la vida en la pandemia de gripe, durante el breve lapso de cinco días, del 15 al 20 de noviembre de 1918».
Eran 80 y el virus mató a 72 en menos de una semana.
Una de las ocho supervivientes era una niña de 12 años. «Murió en 2003, a los 97 años», cuenta su nieta Rita Olanna. «Y sí, claro que mi abuela tenía recuerdos de la gripe española, cómo no iba a tenerlos. La gripe mató a su madre y a todos sus hermanos. Imagine lo que sería eso para una niña: todos esos muertos a la vista, porque no había nadie en condiciones de poder recogerlos. Hubo que esperar a que vinieran de fuera para hacerse cargo de los cadáveres. Ella también tuvo que esperar. Es increíble lo rápida que fue la enfermedad. Un hombre murió tan deprisa que lo encontraron apuntando con su escopeta. A otro lo encontraron sentado en su casa. Increíble. A mi abuela la llevaron a un orfanato de Wales, cerca de aquí. Volvió a Brevig a refundar su familia». Su nieta Rita Olanna tiene ahora 18 nietos, así que la refundación de la familia se puede dar por consumada.
Aforo completo. El alcalde Crockett concluye su presentación y cede el micrófono al más alto de los dos forasteros. «Ése es Johan Hultin, el médico», susurra Rita Olanna. «Mi abuela le ayudó mucho la primera vez que vino. Dios mío, hace ya más de 50 años». Hultin se dirige a la audiencia despacio, con frases cortas y un remoto acento sueco. Como el proyector no funciona, va hilvanando un sencillo discurso de agradecimiento. Les dice a los del pueblo que su colaboración de tantos años ha servido al fin para que el doctor Taubenberger, aquí presente, haya descubierto unas misteriosas pautas remotas: unas pautas que salvarán muchas vidas en el futuro. Les dice que las bases de datos de los científicos acaban de recoger un importante texto genético que se llama Brevig, como su pueblo. Lo dice para que sientan orgullo, pero es su voz la que parece delatarlo: el orgullo reprimido durante medio siglo de un joven médico visionario.
Johan Hultin estudió medicina en Suecia, su país natal, y emigró a Estados Unidos en 1950 con la idea de doctorarse en microbiología por la Universidad de Iowa. Uno de sus profesores mencionó de forma casual que la gripe española había llegado al Ártico, y que entraba en lo posible que el virus permaneciera intacto en el cuerpo de alguna víctima congelada en aquellos hielos perpetuos, el permafrost. El joven Johan, un aventurero con fonendoscopio, vio allí su tema de tesis ideal, extendió un mapa sobre la mesa y no tardó dos segundos en fijarse en Alaska.
Tras consultar a los misioneros que trabajaban con los inupiat, el subgrupo de los esquimales inuit que vive en el lado alasqueño del estrecho de Bering, visitó uno a uno los poblados de la península de Seward buscando cementerios bien asentados sobre el permafrost, donde las tumbas pudieran haber aguantado congeladas incluso en verano, y escuchando historias de viejas sobre aquellas fiebres tan contagiosas como una maldición y tan rápidas que mataban a un hombre mientras apuntaba con su rifle. Cuando vio aquella cruz más alta que las demás en los hielos del cementerio creyó haber hallado al fin la guarida del mayor asesino de la historia. Y su pasaporte hacia la tesis doctoral, allí abajo en Iowa.
54 años después
Ésa fue la primera vez que Hultin visitó Brevig Mission. De nuevo aquí, 54 años después, el médico se ha traído las fotos que hizo entonces. Se las hubiera puesto hoy a los del pueblo durante la charla de haber tenido un proyector, pero de todos modos ha enmarcado las viejas copias de papel para regalárselas al consejo de nativos. Al terminar el acto se acerca a Rita Olanna para enseñarle dos fotos de su abuela, la mujer que murió hace dos años. La conocía muy bien.
En su primera visita, cuando Hultin se reunió con el consejo de nativos y les pidió autorización para excavar en las tumbas, el argumento clave que inclinó la balanza de su lado fue el relato minucioso de los horrores de 1918, que, todavía en 1951, pudieron aportar en esa reunión la abuela de Rita Olanna y otros dos testigos directos. Así lo recuerda Hultin. Y, por lo que Rita Olanna oyó contar a su abuela, las renuencias que hubo en 1951 entre los inuit tuvieron menos relación con la superchería que con la virología. «La gente decía: ‘¿No irá ese médico a resucitar la plaga?».
En realidad, resucitar la plaga era lo único que podía intentar Hultin con las técnicas de la época -ni siquiera se había descubierto la doble hélice del ADN-, y eso fue lo que trató de hacer. El 25 de junio de 1951, ayudado por tres profesores de Iowa, Hultin excavó un par de metros en el permafrost del cementerio de Brevig Mission, encontró cuatro cadáveres con signos evidentes de muerte por hemorragia pulmonar, tomó muestras de varios órganos, las selló en recipientes herméticos y se volvió para Iowa. Usó extractos de las muestras para infectar animales de experimentación, tejidos, células o cualquier otro material que le pudiera permitir rescatar el virus de su letargo de tres décadas, resucitar la plaga que había matado a 50 millones de personas, pero todo falló. Allí no quedaba ni un solo virus. El asesino había muerto. Y Hultin se había quedado sin tesis.
Hoy, 54 años después, Hultin ha vuelto a Brevig Mission. El médico comparte unas alubias con el reportero español en el pulcro comedor de la escuela. En Brevig no hay bares ni hoteles, pero el cocinero Glenn nunca se queda corto de alubias.
-¿Ha venido usted desde España para vernos? -le pregunta Hultin al reportero con sincera sorpresa.
-Pues no, la verdad es que no sabía que venían ustedes.
-Claro, no hemos querido dar publicidad a esta visita.
Es el 6 de diciembre pasado, el termómetro roza los 30 grados bajo cero, el cielo está negro a las tres de la tarde, y el viento, que se merecería una multa de tráfico, hace que la nieve caiga horizontal. Hultin mira por la ventana y le dice al reportero:
-Nosotros nos volvemos a Fairbanks enseguida, antes de que el tiempo se ponga peor.
-Oh, vamos, el tiempo ya no puede ponerse peor.
-¡Ja ja ja! -truena Hultin, fino conocedor de los inviernos de Brevig-. ¿Se aloja usted en la escuela?
-Sólo por esta noche.
-Si se tiene que quedar unos días más, le recomiendo el colchón número dos.
Jefferey Taubenberger sonríe mientras se acaba sus alubias. Poca gente adivinaría que este hombre de aspecto frágil y modales amables dirige una división del Instituto de Patología de las Fuerzas Armadas de Estados Unidos (AFIP), «una de las instituciones más oscuras pero importantes de Washington», según lo ha descrito recientemente The Washington Post. Entre otras muchas cosas, el AFIP practica autopsias a los soldados muertos en las guerras, y su Depósito Nacional de Tejidos archiva tres millones de muestras. Taubenberger tuvo una idea hace 10 años. Cogió el teléfono, marcó la extensión del Depósito de Tejidos y dijo: «Hola, soy Jeff, de Patología Molecular. ¿No tendréis por ahí muestras de alguna víctima de la gripe española?». Había 120.
Junto a la cruz
Cuarenta y cuatro años antes, excavando junto a la cruz de Brevig Mission, el joven Hultin había buscado cadáveres que mostraran evidencias de hemorragia pulmonar, porque así es como actuaba el virus de la gripe española en los casos más limpios, casos sin infecciones bacterianas secundarias que pudieran complicar el cuadro. Aplicando ésa y otras cribas, Taubenberger acabó seleccionando dos muestras de dos soldados muertos por la gripe española el 26 de septiembre de 1918, uno en Carolina del Sur y otro en el Estado de Nueva York. El virus estaba muy deteriorado, pero los científicos consiguieron secuenciar (leer el orden de las letras químicas A, T, G y C) nueve trozos de los genes del virus.
Pese a que sólo era una reconstrucción fragmentaria, se trataba de un logro sin precedentes, y Taubenberger se quitó la bata blanca para redactar un borrador: «Comprender los orígenes del virus de 1918 y los fundamentos de su excepcional virulencia ayudará a predecir las futuras pandemias de gripe…». Cuando salió publicado en Science, el 21 de marzo de 1997, un médico de 73 años afincado en Iowa devoró el artículo de arriba abajo y se dejó caer por el túnel del tiempo hasta los hielos perpetuos de la península de Seward y la cruz de madera de aquel cementerio cercano al fin del mundo. En dos semanas, Johan Hultin estaba otra vez ante el consejo de nativos de Brevig Mission.
«Mi abuela se alegró mucho cuando Hultin volvió, creo que fue en 1997», recuerda Rita Olanna. «Quería excavar otra vez en la fosa. Mi abuela era ya la única superviviente de la gripe española, y el consejo de nativos dio su aprobación enseguida. Hultin volvió en verano. Fue la gente de aquí la que le ayudó a excavar. Encontraron a esa mujer de la que usted habrá oído hablar, una mujer muy gorda».
Hultin sabía que el virus estaba muerto -la inexistencia de su tesis doctoral lo demostraba-, pero se puso unos guantes, sacó del cadáver los pulmones y unas cuantas muestras de otros órganos y se despidió de Brevig Mission por segunda vez. Un par de días después aterrizó en Washington y entregó su tesoro en el AFIP. Taubenberger no encontró allí virus intactos, pero sí muchos fragmentos de sus genes: valiosas piezas para añadir al puzle que apenas había empezado a montar con las muestras de los dos soldados. Le ha costado ocho años, pero ya ha terminado, y ha sido uno de los hitos científicos de 2005. Hace tres meses, dos artículos en Nature y Science sellaban la reconstrucción completa del virus de la gripe española. Casi 90 años después de que la peor pandemia de la historia hubiera matado a 50 millones de personas y desaparecido para siempre, la plaga ha resucitado en un laboratorio de genética. Militar, por supuesto.
No todo el mundo está feliz con el trabajo de Taubenberger. Las comisiones de bioseguridad, los grupos de trabajo sobre armas biológicas y los centros de estudios para la no proliferación -no escasos en Estados Unidos- se han llevado las manos a la cabeza por la «reconstrucción de un virus que tal vez representa el más eficaz agente bioterrorista conocido» (Richard Ebright, Universidad de Rutgers), que sería «extremadamente peligroso si se escapara, y hay una larga tradición de cosas que se escapan» (Barbara Hatch Rosenberg, FAS Working Group on Biological Weapons) y cuya información genética completa, que ya está disponible en bases de datos públicas, «permite a cualquiera encargar a una empresa que se lo fabriquen» (Jonathan Tucker, Center for Nonproliferation Studies, Washington).
Resulta extraño que toda esa trifulca bioterrorista gire en torno a este hombre que se está acabando sus alubias en el comedor de la escuela. ¿No habrá venido aquí a buscar más muestras? ¿Más cadáveres? ¿Virus mutantes?
Nace un asesino
«No, no creo que podamos encontrar nada más en Brevig Mission», responde Taubenberger con una sonrisa. «Sí que me gustaría encontrar alguna muestra de la primera oleada, cuando el virus apareció en la primavera de 1918 y todavía no era mortal. Pero ese virus habrá que buscarlo en otra parte».
El primer caso de gripe española se registró en Camp Funston (Kansas) el 4 de marzo de 1918, y por entonces sólo causaba una dolencia respiratoria leve. Muy contagiosa sí que era, como cualquier gripe, y en abril ya se había propagado por toda Norteamérica, y también había saltado a Europa con las tropas americanas desplazadas al viejo continente. El primer caso de la oleada mortal se registró el 22 de agosto en el puerto francés de Brest, uno de los principales puntos de entrada de los soldados norteamericanos. Era el mismo virus, porque los afectados por la primera oleada estaban inmunizados frente a la segunda. En algún momento del verano, sin embargo, algo lo había convertido en un agente mortal. «Sería muy interesante comparar el virus de la primera oleada con el mortal», dice Taubenberger.
Se sabe que las otras dos pandemias de gripe del siglo XX (1957 y 1968) se originaron cuando un virus de la gripe aviar intercambió genes con un virus de la gripe humana común, y todo el mundo suponía que lo mismo habría ocurrido en 1918. Pero el virus rescatado de los hielos árticos no tiene ningún gen de tipo humano: es un virus de la gripe aviar, sin mezclas. Eso sí, Taubenberger ha descubierto que tiene 25 mutaciones que lo distinguen de un virus de la gripe aviar típico. Entre esas 25 mutaciones deben estar las que le permitieron adaptarse al ser humano.
La pregunta inmediata es si el virus de la gripe aviar actual, el famoso H5N1, que lleva diez años circulando masivamente entre las aves asiáticas, puede sufrir esas mutaciones. Y la respuesta es que ya ha sufrido algunas. Por ejemplo, una de las mutaciones (E627K) halladas en el virus de Brevig Mission reapareció en el virus H5N1 que mató a dos personas en Hong Kong en 1997. Y en cuatro de las seis víctimas analizadas en el brote de Vietnam de 2004. Y en dos de las tres examinadas en Tailandia el mismo año. El virus de la gripe aviar que mató hace tres años a un veterinario en Holanda no era del subtipo H5N1 (sino H7N7), pero llevaba la misma mutación.
¿Estamos presenciando desde la primera fila de butacas una reedición de la catástrofe de 1918?
El virus H5N1
«El virus H5N1 lleva más de diez años circulando entre las aves de China», recuerda Taubenberger, «y millones de chinos han estado expuestos a él sin que se haya producido una pandemia. Eso es tranquilizador. El hecho de que tenga algunas mutaciones en común con el virus de 1918 no parece muy tranquilizador, en cambio. Pero no hemos reconstruido el virus de 1918 para alarmar a nadie, desde luego. La utilidad de este trabajo, creo yo, es que nos ayuda a definir las mutaciones esenciales para que un virus aviar se convierta en una amenaza para la población humana. En el futuro, cuando detectemos parte de esas mutaciones en cualquier control rutinario practicado en aves, sabremos que hay que aplicar ahí las medidas necesarias para detener la evolución del virus».
Raro es el descubrimiento que no trae de regalo un enigma inesperado. Taubenberger sabe ahora que el virus de la gripe española vino de un pájaro, pero no tiene ni la más remota idea sobre qué clase de pájaro pudo ser. Los causantes de las otras dos pandemias (1957 y 1968) eran mezclas, pero su parte aviar provenía claramente de un virus euroasiático. El de 1918 no pertenece a esa familia. Tampoco es un miembro de la otra gran estirpe, la que infecta a las aves del continente americano. Taubenberger es tozudo, y ha llegado a hurgar en la colección del Museo de Historia Natural de Washington hasta dar con 25 aves acuáticas capturadas en 1918, sacarles el virus de la gripe del ano (cloaca, en la jerga) y secuenciar sus genes, que resultaron ser iguales a los de la gripe aviar actual, versión americana. Nada. Entonces, ¿de qué pájaro infernal vino la gripe española?
«Es realmente un misterio», admite Taubenberger. «Estamos colaborando con George Happ, de la Universidad de Alaska en Fairbanks, en un muestreo muy amplio de las aves de Alaska. Nos interesa la evolución de cualquier virus de la gripe aviar, no sólo del H5N1, y tenemos realmente mucho que aprender sobre la ecología de las aves». Ya ven en lo que acaba a veces el dinero del Pentágono.
Hultin y Taubenberger cogieron a tiempo su avioneta a Fairbanks. El tiempo, tal y como dijo Hultin, podía ser aún peor, y el reportero español pudo probar el colchón número dos durante varias noches más de lo previsto. Tres días despúes, el mismísimo alcalde Crockett se ocupó de llevarle a la avioneta. «Gripe aviar, gripe aviar. Cuanto más cambian las cosas, más siguen igual, amigo. No olvide leer a Samuel Huntington». Crockett le ofrece después la mayor prueba de cordialidad que cabe concebir en estas latitudes: quitarse el guante para darle la mano.
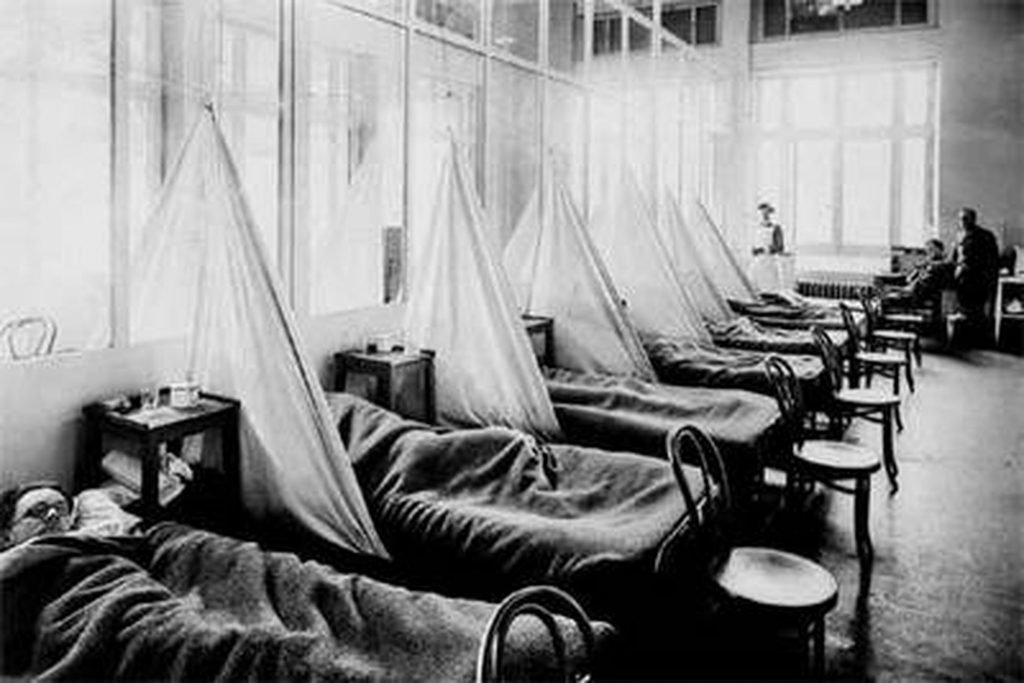
En este solitario cementerio de Brevig Mission (Alaska), el virus de la <b><i>gripe española</b></i> ha guardado su profundo enigma durante más de ochenta años.JAVIER SAMPEDROUn frente aún peor que la guerra. La propagación de la gripe española se vio ayudada por los movimientos de tropas y por el hacinamiento en los hospitales de campaña, como éste del ejército de EE UU en la ciudad francesa de Langres, a finales de 1918.SCIENCE PHOTO LIBRARYLa segunda oportunidad de un visionario. Al leer la reconstrucción parcial del virus que Taubenberger publicó en 1997, Hultin volvió al cementerio de Brevig Mission. Cuando halló el cuerpo de la «mujer gorda», una luz se encendió en su mente. Había esperado ese momento casi medio siglo.J. H.
JUSTA FAMA
LA RESURRECCIÓN del virus de la gripe española no es una simple metáfora. El primer paso sí es una reconstrucción virtual: la secuenciación, o determinación del orden exacto de las letras químicas de los ocho genes del virus. Ni en las dos muestras que Taubenberger seleccionó del depósito de tejidos de Washington ni en la que Hultin extrajo de la víctima del cementerio de Brevig Mission había un solo gen completo, pero no hacía falta. Como había muchos fragmentos que podían secuenciarse, el puzle ha podido recomponerse gracias a los solapamientos entre fragmentos. El resultado son ocho ristras de A, T, G y C escritas en un papel, o introducidas en la memoria de un ordenador, que representan los ocho genes del virus de 1918. Hasta ahí la reconstrucción virtual.
Pero la técnica actual permite convertir una secuencia escrita en un papel en un gen de verdad. Basta ir pegando los compuestos químicos (bases) A, T, G y C uno a uno en el orden que dicta la secuencia de papel. Un virus es algo más que sus genes: tiene una cubierta que rodea los genes y se encarga de infectar las células humanas. Pero una de las funciones de los genes es precisamente fabricar esa cubierta, de modo que, teniendo la secuencia de papel, los científicos ya saben, literalmente, resucitar el virus. Y lo han hecho.
Han podido comprobar así que el virus de la gripe española se multiplica 50 veces más que la gripe común tras un día de infección, y 39.000 veces más tras cuatro días, y que mata a todos los ratones de laboratorio en menos de una semana.
* Este artículo apareció en la edición impresa del sábado, 07 de enero de 2006.



